贝利尤单抗和阿尼鲁单抗及泰它西普治疗系统性红斑狼疮疗效和安全性的网状Meta分析
系统性红斑狼疮(systemic lupus erythematosus,SLE)是一种慢性多系统自身免疫性疾病,可导致人体几乎所有主要器官受累[1]。全球SLE的患病率为(20~150)/10万[2-3]。近几十年来,得益于早期诊断和治疗,SLE患者生存率显著提高[4-6]。目前研究证明常规药物治疗SLE有效[7-8],包括激素、抗疟药和免疫抑制剂。然而,SLE患者的一些需求仍未得到满足,包括对于疾病持续活跃、无法控制或反复发作的患者需要长期使用类固醇和免疫抑制剂治疗,导致器官进行性损伤、生活质量差、感染率增加、经济负担重[9-11],且长期预后差,死亡率较同龄人群高2~5倍,年复发率为每例患者0.19~1.20次/年[12]。有证据表明,疾病持续活跃、类固醇使用和进行性器官损伤会增加SLE患者的死亡风险[13-16];传统治疗药物具有广泛的免疫抑制机制,可引起不同程度的不良反应[7-8],基于这些原因,研究者们仍在不断研究开发新的治疗策略用于治疗SLE,目前生物制剂治疗SLE被证明疗效显著,迄今为止,已有3种生物制剂被多个国家批准用于SLE治疗[17-20],分别为贝利尤单抗、阿尼鲁单抗、泰它西普。
虽然,目前研究表明3种新型生物制剂作为标准治疗的附加疗法用于治疗SLE较安慰剂组有效,但目前尚缺乏直接比较3种药物疗效及安全性的研究。在没有直接比较的试验的情况下,本研究采用网状Meta分析方法间接比较3种药物的有效性及安全性。
1 资料与方法
1.1 文献检索策略
通过检索PubMed、Web of Science、Cochrane Library、Embase数据库中有关贝利尤单抗、阿尼鲁单抗、泰它西普治疗SLE的随机对照试验(randomized controlled trial,RCT),以主题词+自由词进行检索,英文检索词为“Lupus Erythematosus,Systemic”“anifrolumab”“telitacicept”“randomized controlled trial”。检索时间为建库至2023年8月。以PubMed检索策略为例。
1.2 文献纳入与排除标准
1.2.1 纳入标准:(1)研究对象:符合诊断标准的SLE患者。(2)干预措施:①贝利尤单抗10 mg/kg静脉注射;②贝利尤单抗200 mg皮下注射;③阿尼鲁单抗300 mg静脉注射;④泰它西普160 mg皮下注射;⑤安慰剂+标准治疗(皮质类固醇、抗疟药、免疫抑制剂等)。(3)研究类型:RCT。(4)疗效及安全性结局指标:①SLE应答指数4(SLE responder index 4,SRI4);②严重复发率(severe flare,SF);③皮质类固醇剂量减少:基线时接受类固醇剂量>7.5 mg/d治疗的患者在研究终点时减少≥25%且≤7.5 mg/d的患者比例(贝利尤单抗),基线时接受口服类固醇>10 mg/d治疗的患者剂量减少至7.5 mg/d(阿尼鲁单抗);④总不良事件(total adverse events,TAEs)(至少出现1次)、严重不良事件(serious adverse events,SAEs)及常见不良事件的发生率。
1.2.2 排除标准:(1)以SLE相关疾病或并发症为研究对象,如狼疮性肾炎、狼疮性脑病、妊娠期SLE、皮肤狼疮等;(2)非RCT;(3)干预措施和结局指标不符合纳入标准;(4)重复发表、数据不全、正在进行的研究。
1.3 文献质量评价
采用Cochrane协作工具进行偏倚风险评估,包括以下7个项目:序列生成、分配隐藏、结果评价、不完整的结果数据、受试者和参与人员双盲、选择性报告和其他潜在偏倚来源,每个项目评为“低风险”“不清楚”“高风险”。
1.4 文献筛选与数据提取
2名独立的研究人员严格按照纳入与排除标准对检索的全部文献进行筛选与数据提取。结果对比有差异时,寻求第3位研究人员共同进行决策。研究数据的提取内容包括第一作者、出版年份、国家、干预措施、样本量、年龄、疗程、结局指标等。
1.5 统计学方法
采用RevMan 5.4.1软件进行直接Meta分析,研究间的异质性采用I2值检验,若I2≤50%,认为同质性良好,选择固定效应模型合并效应值;若I2>50%,则认为存在异质性,采用随机效应模型合并效应值。计数资料采用比值比(odds ratio,OR)和95%置信区间(confidence interval,CI)表达效应量,P<0.05表示差异有统计学意义;绘制发表偏倚漏斗图,评估发表偏倚;采用R 4.3.1绘制证据关键网络图。
采用ADDIS 1.16.8软件进行贝叶斯网状Meta分析,该软件基于贝叶斯框架,使用马尔科夫链蒙特卡罗(MCMC)方法完成数据处理、统计,设置4条马尔科夫链,初始值为2.5,退火迭代20 000,模拟迭代50 000次,细化迭代10次。由于本研究证据关系网络图不存在闭合环,因此选用一致性模型进行贝叶斯网状Meta分析及排序,收敛性采用潜在尺度缩减因子(potential scale reduced fctor,PSRF)评价,PSRF趋向1表明收敛性较好、一致性模型分析结论稳定,真实性较高;通过累积概率排序图进行药物优劣排序。
2 结果
2.1 纳入文献的基本特征
初检共获得3 600篇文献,排除重复文献后获得1 916篇,经阅读题目、摘要、全文后共纳入12篇文献[21-32];共纳入研究对象4 789例,其中试验组2 721例,对照组2 068例。
2.2 纳入文献的质量评价
采用Cochrane工具评估偏倚风险评价纳入的研究,纳入文献质量评价高。
2.3 直接Meta分析
2.3.1 贝利尤单抗与安慰剂
2.3.1.1 有效性:有6篇研究[22-25,29-30]以52周SRI4缓解率为结局指标,各研究间无统计学异质性(I2=0,P=0.89),采用固定效应模型进行Meta分析,结果显示,贝利尤单抗组SRI4缓解率高于安慰剂组,差异有统计学意义(OR=1.62,95%CI=1.40~1.88,P<0.001)。
有5篇研究[22-25,30]以52周SF为结局指标,各研究间无统计学异质性(I2=0,P=0.55),采用固定效应模型进行Meta分析,结果显示,贝利尤单抗组SF低于安慰剂组,差异有统计学意义(OR=0.59,95%CI=0.49~0.71,P<0.001)。
有4篇研究[22-24,30]以皮质类固醇剂量减少所占比例为结局指标,各研究间无统计学异质性(I2=0,P=0.91),采用固定效应模型进行Meta分析,结果显示,贝利尤单抗组皮质类固醇剂量减少所占比例高于安慰剂组,差异有统计学意义(OR=1.48,95%CI=1.09~2.02,P<0.001)。
按照给药方式进行亚组分析,根据试验组贝利尤单抗给药方式的不同分为贝利尤单抗(静脉注射)亚组和贝利尤单抗(皮下注射)亚组,Meta分析结果显示,贝利尤单抗(静脉注射)亚组和贝利尤单抗(皮下注射)亚组的SRI4缓解率均高于安慰剂组,差异有统计学意义(OR=1.59,95%CI=1.35~1.89,P<0.001;OR=1.69,95%CI=1.27~2.27,P<0.001)。贝利尤单抗(静脉注射)亚组和贝利尤单抗(皮下注射)亚组的SF均低于安慰剂组,差异有统计学意义(OR=0.60,95%CI=0.49~0.75,P<0.001;OR=0.53,95%CI=0.35~0.80,P=0.002)。
2.3.1.2 安全性:共7项研究[21-25,29-30]报道有关贝利尤单抗治疗的不良事件,报道不良事件数据完整,各研究间无统计学异质性(I2=0,P=0.95),采用固定效应模型进行Meta分析,结果显示,贝利尤单抗组和安慰剂组TAEs发生率比较,差异无统计学意义(OR=0.89,95%CI=0.72~1.08,P=0.24)。
按照给药方式进行亚组分析,根据试验组贝利尤单抗给药方式的不同分为贝利尤单抗(静脉注射)亚组和贝利尤单抗(皮下注射)亚组,Meta分析结果显示,贝利尤单抗(静脉注射)亚组和贝利尤单抗(皮下注射)亚组分别与安慰剂组TAEs发生率比较,差异均无统计学意义(OR=0.93,95%CI=0.73~1.18,P=0.55;OR=0.78,95%CI=0.53~1.15,P=0.21)。
贝利尤单抗组和安慰剂组SAEs发生率比较,差异无统计学意义(OR=0.82,95%CI=0.59~1.12,P=0.25);常见不良反应如上呼吸道感染、尿路感染、腹泻、头痛、关节痛、咳嗽、恶心、鼻咽炎、鼻窦炎发生率,贝利尤单抗组和安慰剂组比较,差异均无统计学意义(P>0.05)。
2.3.2 阿尼鲁单抗与安慰剂
2.3.2.1 有效性:有2篇研究[26,31]以52周SRI4缓解率为结局指标,各研究间无统计学异质性(I2=11%,P=0.29),采用固定效应模型进行Meta分析,结果显示,阿尼鲁单抗组SRI4缓解率高于安慰剂组,差异有统计学意义(OR=2.39,95%CI=1.70~3.37,P<0.001)。
有3篇研究[26-27,31]以52周SF为结局指标,各研究间无统计学异质性(I2=0,P=0.43),采用固定效应模型进行Meta分析,结果显示,阿尼鲁单抗组SF低于安慰剂组,差异有统计学意义(OR=0.52,95%CI=0.39~0.69,P<0.001)。
有3篇研究[26-27,31]以52周皮质类固醇剂量减少所占比例为结局指标,各研究间无统计学异质性(I2=0,P=0.48),采用固定效应模型进行Meta分析,结果显示,阿尼鲁单抗组皮质类固醇剂量减少所占比例高于安慰剂组,差异有统计学意义(OR=2.45,95%CI=1.69~3.54,P<0.001)。
2.3.2.2 安全性:共3项研究[26-27,31]报道有关阿尼鲁单抗治疗后的不良事件,各研究间无统计学异质性(I2=0,P=0.50),采用固定效应模型进行Meta分析,结果显示,阿尼鲁单抗组TAEs发生率高于安慰剂组,差异有统计学意义(OR=1.80,95%CI=1.25~2.59,P=0.001)。
阿尼鲁单抗组SAEs发生率(OR=0.67,95%CI=0.46~0.97,P=0.04)、上呼吸道感染发生率(OR=1.76,95%CI=1.19~2.60,P=0.005)、鼻咽炎发生率(OR=1.82,95%CI=1.23~2.70,P=0.003)、支气管炎发生率(OR=2.31,95%CI=1.35~3.94,P=0.002)、带状疱疹发生率(OR=4.26,95%CI=1.84~9.85,P<0.001)均高于安慰剂组,差异有统计学意义;两组尿路感染、头痛发生率比较,差异均无统计学意义(P>0.05)。
2.3.3 泰它西普与安慰剂
2.3.3.1 有效性:有2篇研究[28,32]以SRI4缓解率评价疗效,各研究间存在统计学异质性(I2=56%,P=0.13),采用随机效应模型进行Meta分析,结果显示,泰它西普组SRI4缓解率高于安慰剂组,差异有统计学意义(OR=6.28,95%CI=3.20~12.33,P<0.001)。
2.3.3.2 安全性:有2篇研究[28,32]报告泰它西普治疗后TAEs发生率,各研究间无统计学异质性(I2=0,P=0.74),采用固定效应模型进行Meta分析,结果显示,泰它西普组TAEs发生率高于安慰剂组,差异有统计学意义(OR=2.13,95%CI=1.18~3.83,P=0.01)。一项Ⅲ期研究结果,泰它西普组SAEs发生率低于安慰剂组[12例(7.2%)与24例(14.3%)][32],常见的不良事件是上呼吸道感染、血液免疫球蛋白(Ig)G和IgM降低、注射部位不良反应和尿路感染。
2.4 间接Meta分析
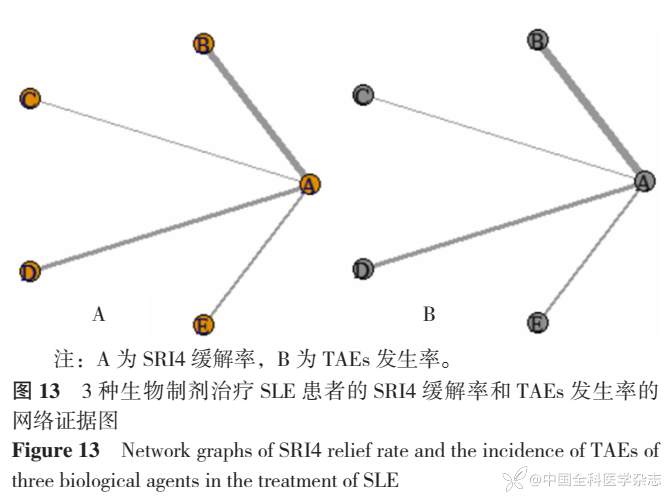
2.4.1 网络证据图:纳入10项研究[22-26,28-32]有关SRI4缓解率的网络证据图见图13,纳入12项研究[21-32]有关TAEs发生率的证据关系网络图见图13;图中的节点表示干预措施,节点大小表示纳入样本量的大小,节点之间的连接线,表示直接比较关系,实线的粗细表示纳入研究的数量。
2.4.2 一致性模型分析:由于本研究证据关系网络图不存在闭合环,因此选用一致性模型进行贝叶斯网状Meta分析及排序,收敛性采用PSRF评价,PSRF为1.00~1.01,表明收敛性较好、一致性模型分析结论稳定,真实性较高。
2.4.3 SRI4:有10篇研究[22-26,28-32]以SRI4缓解率为结局指标,贝叶斯网状Meta分析结果显示,试验组干预措施为贝利尤单抗(静脉注射)、贝利尤单抗(皮下注射)、阿尼鲁单抗、泰它西普的SRI4缓解率均高于安慰剂组,差异有统计学意义(P<0.05)。试验组干预措施为贝利尤单抗(静脉注射)、贝利尤单抗(皮下注射)、阿尼鲁单抗的SRI4缓解率均低于泰它西普,差异有统计学意义(P<0.05)。其他干预措施试验组两两间接比较,差异均无统计学意义(P>0.05);3种生物制剂的SRI4缓解率的概率排序为泰它西普>阿尼鲁单抗>贝利尤单抗(皮下注射)>贝利尤单抗(静脉注射)。
2.4.4 TAEs:纳入文献中有12篇研究[21-32]以TAEs发生率为结局指标,贝叶斯网状Meta分析结果显示,试验组干预措施为阿尼鲁单抗、泰它西普的TAEs发生率高于安慰剂组,差异有统计学意义(P<0.05);贝利尤单抗静脉注射和皮下注射相较于安慰剂组的TAEs发生率,差异无统计学意义(P>0.05);不同干预措施的试验组患者TAEs发生率比较,阿尼鲁单抗组TAEs发生率高于贝利尤单抗静脉注射组和皮下注射组,差异有统计学意义(P<0.05);贝利尤单抗静脉注射组和皮下注射组TAEs发生率低于泰它西普组,差异有统计学意义(P<0.05);其他干预措施试验组TAEs发生率两两间接比较,差异均无统计学意义(P>0.05);3种不同药物及不同用药方式TAEs发生率的概率排序为泰它西普>阿尼鲁单抗>贝利尤单抗(静脉注射)>贝利尤单(皮下注射)。
2.5 发表偏倚
纳入12篇研究将TAEs发生率作为结局指标,绘制漏斗图散点多分布于中上部,左右对称,提示TAEs发生率的文献发表偏倚可能性小。
3 讨论
对于SLE,人们越来越认识到持续的疾病活动性和较高的糖皮质激素剂量是器官损伤的主要预测因素[13,33]。因此,以尽可能低的糖皮质激素剂量实现疾病活动性控制是目前重要的治疗目标[10]。本研究结果显示,贝利尤单抗、阿尼鲁单抗、泰它西普3种药物作为标准治疗的附加疗法相较于安慰剂加标准治疗显示出了良好的临床治疗效果,使中至重度SLE患者SRI4缓解率明显提升,表明3种药物与SLE患者的疾病活动性降低、预后改善相关,贝利尤单抗、阿尼鲁单抗相较于安慰剂实现了减少糖皮质激素剂量、降低疾病复发率,进而延缓器官损害进展、提高生活质量等优点;根据不同生物制剂改善SLE患者的SRI4缓解率的累积概率排序图进行排序,疗效从高到低依次为泰它西普、阿尼鲁单抗、贝利尤单抗(皮下注射)、贝利尤单抗(静脉注射)。贝叶斯网状Meta分析显示,泰它西普疗效优于贝利尤单抗和阿尼鲁单抗,而后两者疗效差异似乎不明显;因SLE疾病机制的复杂性,未有任何一种生物制剂对SLE显示出百分之百的疗效,因此对于SLE的治疗,可能需要在一种生物制剂显示疗效不佳或疾病再次复发时,及时更换另一种不同机制的生物制剂进行继续治疗,甚至可能需要多种不同机制的生物制剂联合治疗。本研究的3种生物制剂,对于SLE累及其他系统引起的疾病似乎也有疗效,已有明确的证据证实贝利尤单抗在狼疮肾炎和儿童SLE的疗效,基于FURIE等[34]的结果,美国食品药品监督管理局(FDA)批准贝利尤单抗用于治疗活动性狼疮性肾炎和儿童SLE[35];也有研究提示阿尼鲁单抗和泰它西普治疗狼疮肾炎和儿童SLE有改善疗效的作用,尤其是泰它西普更有可能被批准;目前尚未有任何生物制剂被批准用于皮肤狼疮(CLE),但已有多个发表的病例研究和小样本观察研究表明,贝利尤单抗、阿尼鲁单抗、泰它西普可能在治疗难治性CLE成为潜在的选择[20]。
本研究直接Meta分析显示,使用贝利尤单抗静脉注射或皮下注射与安慰剂组的TAEs发生率相似,贝利尤单抗静脉注射组相较于安慰剂组SAEs发生率并无差异,且常见不良反应如上呼吸道感染、尿路感染、腹泻、头痛、关节痛、咳嗽、恶心、鼻咽炎、鼻窦炎发生率相较于安慰剂组也并未显示明显差异;使用阿尼鲁单抗或泰它西普治疗组的TAEs发生率略高于安慰剂组,虽然阿尼鲁单抗相较于安慰剂可降低SAEs发生率,但也增加了一些常见不良反应发生率,如上呼吸道感染、鼻咽炎、支气管炎、带状疱疹,其中以带状疱疹发生率增加最为显著;其他常见不良反应发生率,如尿路感染、头痛发生率并未有差异;虽然仅有1篇纳入研究报告了SAEs发生率,但结果显示泰它西普似乎可以降低SAEs发生率,并且使用泰它西普的患者出现常见的不良事件是上呼吸道感染、血液IgG和IgM降低、注射部位不良反应和尿路感染[32]。贝叶斯网状Meta分析显示,根据不同生物制剂治疗SLE出现的TAEs发生率的累积概率排序图进行排序,从高到低依次为泰它西普、阿尼鲁单抗、贝利尤单抗(静脉注射)、贝利尤单抗(皮下注射);直接Meta分析与间接Meta分析结果一致。虽然使用泰它西普和阿尼鲁单抗的不良事件发生率高于贝利尤单抗,但对于降低SAEs发生率前两种药似乎更有优势。既往研究表明,长期使用贝利尤单抗或阿尼鲁单抗依然有持续稳定的安全性[36-38],在一项研究贝利尤单抗治疗的SLE患者长达8年的安全性研究中显示[36],每年常见不良事件、SAEs发生率保持稳定甚至下降。另一项为期3年的阿尼鲁单抗治疗SLE患者的研究,表明阿尼鲁单抗具有可接受的长期安全性。
本研究局限性:(1)虽然本研究严格执行网状Meta分析步骤,但目前尚无直接比较3种药物的疗效及安全性的研究,因此本研究的结论尚有待进一步的证实;(2)本研究纳入文献并未提及泰它西普治疗后关于皮质醇激素减量方面的数据,因此不能间接表明3种药物关于该方面的结论;(3)因研究阿尼鲁单抗与贝利尤单抗关于皮质醇激素减量、严重复发评价指标有所差异,为避免结果偏倚,未进行贝叶斯Meta分析。
综上所述,贝利尤单抗、阿尼鲁单抗、泰它西普治疗中重度SLE患者均有明显的疗效,其中泰它西普的疗效最为显著;贝利尤单抗和阿尼鲁单抗的应用可降低口服激素剂量、减少疾病复发可能,从而减少激素的不良反应,提高患者生活质量,泰它西普似乎也有类似的优点,但仍需进一步的数据支持。使用泰它西普、阿尼鲁单抗的患者在临床缓解率和SAEs发生率方面可能优于贝利尤单抗,但贝利尤单抗并未增加不良事件发生率。
参考文献略
















































