溶出终点达不到85/80怎么办?
《溶出度技术试验技术》一书中,开篇序言中提到这么一句话:对于普通口服固体制剂,只要是存在生物不等效的产品,产品间就不会不表现溶出度方面的显著差异性。
这句话体现了溶出度的考察在制剂研究中的重要地位,这里的显著性差异应该来自于具有区分力的溶出条件,对于最具有区分力应该是那条传说中可建立IVIVC的溶出曲线。
但是,对于IVIVC普通口服固体制剂通常 是难以建立的,新药开发过程中往往是基于临床试验中多次试验通过药代动力学参数建立与体外溶出曲线的关联性。
对于仿制药,建立IVIVC在目前的大环境下更是难上加难。因此体外溶出曲线的研究,对于仿制药的开发起着不可替代的作用,在一定的前体下,仿制药的溶出曲线与原研产品越相似,那么通过Be的概率也越大。
非模型依赖法(f2 )相似因子的比较在溶出曲线相似性的比较过程中的应用较多,《普通口服固体制剂溶出曲线测定与比较指导原则》中对于采用相似因子(f2)法比较溶出曲线相似性的要求:
(1)时间点的选取应尽可能以溶出量等分为原则,并兼顾整数时间点,且溶出量超过85%的时间点不超过1个。
(2)第1个时间点溶出结果的相对标准偏差不得过20%,自第2个时间点至最后时间点溶出结果的相对标准偏差不得过10%。
对于制剂的相对标准偏差超出f2的适用范围,可采用非模型依赖多变量置信区间法进行处理。
那么问题来了,在实际研发过程中我们经常会遇到参比制剂的累积溶出度小于85%的情况,指导原则中有这么一句话:当溶出曲线不能采用相似因子(f2)法比较时,可采用其他适宜的比较法,但在使用时应给予充分论证。我们先看一个2015版药典收载品种甲睾酮片的溶出方法:

FDA溶出度数据库收载的溶出方法:
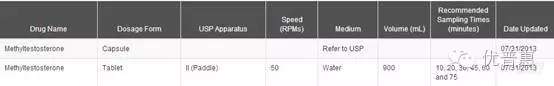
PMDA收载的溶出方法:

对比看出,咱们的处理方式有两宝:加大转速和加入有机溶剂。制剂的溶出不好,在一定程度上会影响药物的临床疗效。这也可能造就历史上某种制剂只要成型就行,制剂谁都能做好的局面。
以下为在制剂开发过程中遇到的一些具体实例:
实例1:参比制剂在不同pH介质中的溶出曲线(100rpm)
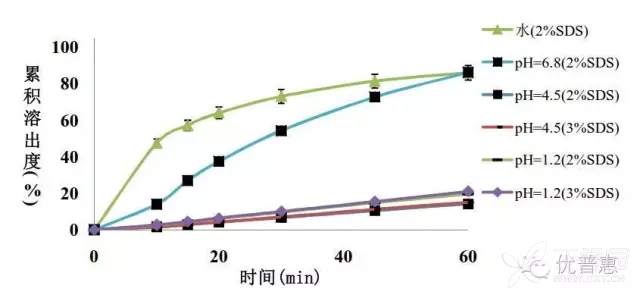
实例2:自制制剂与参比制剂在pH=6.8(含0.5%表活-75rpm)介质中的曲线对比
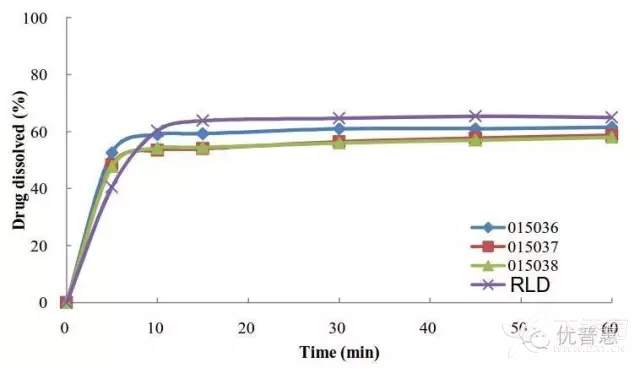
实例3:不同转速下参比制剂的溶出曲线
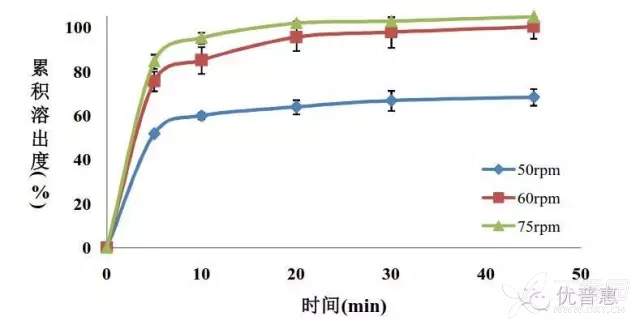
当然,在一定条件下加快转速可能加快溶出,但也可能造就溶出的条件完全没有区分力,任何一个处方工艺都能达到溶出度要求,这样会造成假阳性的结果。比如含有磷酸钙的产品,如“络活喜”,溶出时磷酸钙会沉淀于杯底,转速过低可能会区分过渡,造成假阴性的结果。为此对于实例1、2和3适宜的溶出条件下,相似性的比较可参考《日本生物等效性试验指导原则》,作者已有采用此相似性比较方法成功申报过制剂的案例,具体判断依据如下:
1、参比制剂平均溶出率在规定时间内达50%以上但未达85%时,选取参比制剂平均溶出率的1/2所对应的时间点和最终时间点,两者平均溶出率的差均在±12%范围内。
2、参比制剂平均溶出率在规定时间内达不到50%时,选取参比制剂平均溶出率的1/2所对应的时间点和最终时间点,两者平均溶出率的差均在±9%范围内。但是,规定试验时间内,参比制剂的平均溶出率低于10%时,只以规定试验时间作为评价手段,两者平均溶出率差在±9%范围内。
对比缓释制剂的判断依据如下(释放机制一致,以缓释24h为考察终点):
1、参比制剂在规定时间内平均溶出率达50%以上但未达到80%时,选取最终时间点和参比制剂在最终时间点的平均溶出率为1/2时所对应的时间点,两者平均溶出率的差均在±12%范围内。
2、参比制剂在规定时间内平均溶出率达不到50%时,选取最终时间点和参比制剂在最终时间点的平均溶出率为1/2时所对应的时间点,两者平均溶出率的差均在±9%范围内。但是,规定试验时间内,参比制剂的平均溶出率低于10%时,只以规定试验时间作为评价手段,两者平均溶出率差在±9%范围内。
作者:汤晨懿
















































